수소-선택적인 환원촉매의 알칼리 금속 담지에 따른 질소산화물과 일산화탄소 저감에 미치는 영향
초록
이 연구는 H2-SCR의 상용화를 위한 기초 연구로 산성 계열인 질소산화물의 흡장 물질인 알칼리 금속이 담지될 때 유해가스 저감에 미치는 영향을 파악하는 것이다. 2Ag/Al2O3(STD) H2-SCR의 BET 비표면적은 180.41 m2/g으로 알칼리 금속이 담지된 세 종류 H2-SCR보다 BET 비표면적이 컸다. 2Ag/Al2O3(STD) H2-SCR은 약 260℃에서 환원되는 피크가 발생했고, AgO은 산화물에서 Agnδ+로 환원되었다. Ag 클러스터(Agnδ+)는 AgO 산화물 보다 불안정한 상태이므로, Ag의 촉매의 화학 반응을 촉진시켰다. 2Ag/Al2O3(STD) H2-SCR은 100℃에서 약 27%의 NOx 전환율을 나타냈고, 알칼리 금속이 담지된 세 종류 H2-SCR보다 저온에서 활성화 되었다. H2-SCR은 알칼리 금속에 담지에 따라 저온에서 활성은 향상되지 않았지만, 내연기관의 배출가스 온도에 따라 적절한 조촉매 물질 담지를 통하여 유해가스 저감 성능의 window는 조정할 수 있다.
Abstract
This study is fundamental research for the commercialization of H2-SCR to identify the effect on reducing harmful gases when alkali metals, which are storage materials for acidic nitrogen oxides, are loaded. The BET specific surface area of 2Ag/Al2O3 (STD) H2-SCR was 180.41 m2/g, which was larger than that of the three types of H2-SCRs loaded by alkali metals. 2Ag/Al2O3 (STD) H2-SCR had a reduction peak at about 260℃, and AgO was reduced from oxide to Agnδ+. Since the Ag cluster (Agnδ+) is more unstable than AgO oxide, it promoted the chemical reaction of the Ag catalyst. 2Ag/Al2O3 (STD) H2-SCR showed a NOx conversion rate of about 27% at 100°C and was activated at lower temperatures than the three types of H2-SCR loaded with alkali metal. H2-SCR did not improve its activity at low temperatures as it was loaded on alkali metals, but the window of harmful gas reduction performance could be adjusted by supporting appropriate additive catalyst materials according to the exhaust temperature of the internal combustion engine.
Keywords:
Hydrogen, Selective Catalytic Reduction, NOx, Carbon Monoxide, Alkali Metal키워드:
수소, 선택적환원촉매, 질소산화물, 일산화탄소, 알칼리 금속1. 서 론
최근에 이상고온, 열대야, 한파, 호우, 폭설, 가뭄 등 이상기후가 빈번하게 발생하고 있으며, 이러한 이상기후는 화석에너지원의 사용 비중이 높기 때문이다. 탄소 중립 정책이 세계적인 이슈로 급부상하고 있으며,1) 그 대책의 일환으로 전기자동차(EV), 연료전지전기자동차(FCEV)로 친환경에너지로 전환이 진행되고 있다. 최근에는 전기자동차의 보급률이 주춤하고 있으며, 전기자동차의 높은 가격과 인프라 부족 및 하이브리드 전기자동차(Hybrid Electric Vehicle) 판매가 증대하고 있기 때문이다. EC(European Commission)는 Euro 7 배기가스 규정을 제안하였고, 새로운 경 차량에 대해서는 2025년도 7월 1일에, 대형 차량에 대해서는 2027년 7월 1일에 발효된다.2) 특히, 질소산화물(NOx)은 내연기관에서 배출량이 많으며 세계보건기구(World Health Organization, WHO)에서 정한 발암물질이다.3) 현재까지 NOx 저감을 위한 엔진 전처리 장치로는 EGR(Exhaust Gas Recirculation) 시스템과 후처리 장치는 SCR(Selective Catalytic Reduction)4,5) 시스템이 있다.
현재 CO2 배출이 없는 수소(H2)가 각광을 받고 있으며, 수소는 다양한 분야로 활용이 가능하다. 최근에는 H2-엔진이 개발되었고, 배출될 수 있는 가스는 NOx와 H2O이다. 또한 배출 가스 온도가 낮은 가정용 보일러 등에 수소는 활용 범위가 넓다.
수소 환원제를 이용하여 유해 가스를 저감시키는 SCR 촉매를 H2-SCR이라고 한다. 지금까지의 연구 동향은 환원제 H2 이용하여 NOx 저감 성능을 향상시키는 연구가 진행되어 왔다. H2-SCR 촉매의 성능 향상을 위해 주촉매(main catalyst)6), 안정제(promoter)7,8), 지지체(support)99,10) 및 반응 메커니즘 등에 관한 선행 연구가 이루어져 왔다. 그러나 순수 H2-SCR 촉매에 사용되는 귀금속은 Pt와 Pd를 다용하는 추세이며, 이는 촉매 비용이 증가하므로 경제성을 고려한 Ag 기반 H2-SCR 촉매에 NOx 흡장 물질인 알칼리 금속(Ba, Ca, Na) 담지에 대한 영향에 관한 연구는 부족하며, 의의가 있다.
이 연구는 Ag 기반 H2-SCR에 알칼리 금속 담지가 유해가스 저감 성능에 미치는 영향을 파악하는 것이다.
2. 촉매 제조 및 실험 방법
제조된 H2-SCR은 합침법(impregnation method)으로 제조되었다. 함침법은 지지체를 활성 물질이 녹아 있는 용액에 담근 후 용매를 증발시켜 활성 물질을 지지체에 담지하는 방법이다. 500 cc 비이커에 증류수 300 cc를 붓고, 총량 기준으로 지지체 88 wt%의 Al2O3를 넣는다. 2 wt%의 Ag를 넣고 3시간 동안 교반하였다. 마지막으로 3종류 알칼리 금속(Ba, Ca, Na) 10 wt%를 넣고 3시간 동안 교반하였다. H2-SCR은 400CPSI(Cell Per Square Inch) 담체(substrate)에 198g/L을 코팅하였다. 500℃에서 3시간 동안 공기로 소성(calcination)하였고, 400℃에서 1시간 H2 5%로 환원(reduction) 처리하였다.
Table 1은 H2-SCR의 de-NOx/CO 성능 평가를 위한 모델가스 조건이다. 모델가스반응장치는 가스 공급부, 유량 제어부, 촉매 반응부 및 분석부로 구성된다. 촉매 온도는 75∼350℃ 정상상태(steady state) 조건에서 5분을 유지하면서 de-NOx/CO 성능을 측정하였다. H2-SCR의 유해 가스 정화 성능은 아래 식 (1)과 같이 계산하였으며, 촉매 반응 후의 가스 성분은 MRU 가스분석기(VarioPlus Industrial, MRU Instruments, Inc.)를 이용하여 1초 간격으로 정량적으로 측정하였다.
| (1) |
3. 실험 결과 및 고찰
3.1 H2-SCR의 알칼리 금속 담지에 따른 물리·화학적 특성
알칼리 금속(Ba, Ca, Na)은 최외각 전자 껍질의 전자 하나를 쉽게 잃어 +1 전하를 가진 양이온을 이룬다. 알칼리 계열이므로 산성 계열인 질소산화물(NOx)과 화학 반응성이 좋으므로 NOx 흡장 물질로도 사용되어져 왔다. 이 절에서는 알칼리 금속이 H2-SCR 촉매에 담지될 때의 물리·화학적인 특성을 파악하고자 한다.
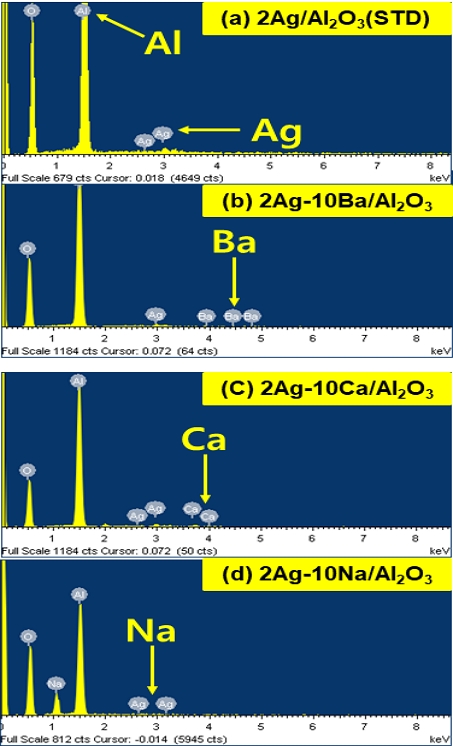
Fig. 1은 H2-SCR의 알칼리 금속 담지에 따른 SEM 및 TEM 이미지이다. 촉매의 2차원 표면 분석은 주사전자현미경인 SEM(JSM-7500F+EDS, Oxford) 분석기를 이용하였다. H2-SCR에 포함된 물질의 형상과 사이즈를 분석하기 위해 TEM(JEM-2000FXⅡ(200kV), JEOL)을 이용하였다. Fig. 1(a)에서 활성 물질인 Ag와 알칼리 금속(Ba, Ca, Na)의 결정은 구분하기는 쉽지 않다. 지지체 알루미나(Al2O3)의 결정 입자의 폭은 10 nm보다 작고, 길이는 약 15∼60 nm 사이즈로 직사각형의 형상을 하고 있다. SEM 이미지에서 명암 차이는 샘플이 뛰어나옴에 따라 전자가 누적된 “Charge-up” 현상이다. Fig. 1(b)의 TEM 이미지에서 알루미나 결정은 투명하게 확인이 가능하다. Fig. 1(b-4)의 2Ag-10Na/Al2O3 샘플에서 약 100 nm급의 응집된 입자는 나트륨 산화물(NaO)로 판단이 되며, 반응이 좋은 나트륨이 촉매 제조 중에 산화물로 크게 자리 잡고 있다. Fig. 2는 알칼리 금속 담지에 따른 H2-SCR 촉매의 SEM-EDX 자료이다. Fig. 2의 (a)∼(d)에서 지지체 Al2O3, 활성물질 Ag 및 세 종류 알칼리 금속(Ba, Ca, Na)이 10 wt% 포함되었을 때 주 피크와 보조 피크가 잘 생성되어 있다.
Table 2는 알칼리 금속이 담지된 H2-SCR의 BET 비표면적 등 물리적인 특성을 나타내고 있다. 2Ag/Al2O3(STD) H2-SCR은 BET 비표면적이 180.41 m2/g으로 알칼리 금속이 담지된 세 종류 H2-SCR보다 BET 비표면적이 크다. Ba와 Ca가 담지된 H2-SCR은 BET 비표면적과 Pore size와 Pore volume 차이는 크지 않으나, 알칼리 금속이 담지 않은 2Ag/Al2O3(STD) H2-SCR보다 BET 비표면적과 Pore volume 값은 작아지는 경향을 나타내고 있다. 그러나 2Ag-10Na/Al2O3 H2-SCR은 BET 비표면적이 107.44 m2/g으로 2Ag/Al2O3(STD) H2-SCR 보다 44.44% 감소하였고, Pore volume 또한 0.32 cm3/g으로 61.44% 감소하였다. BET 비표면적과 Pore volume이 작아지면 촉매가 흡착-반응-탈착할 수 있는 활성사이트(Active site)가 작아짐에 따라 촉매의 성능에 영향을 미칠 수 있다.
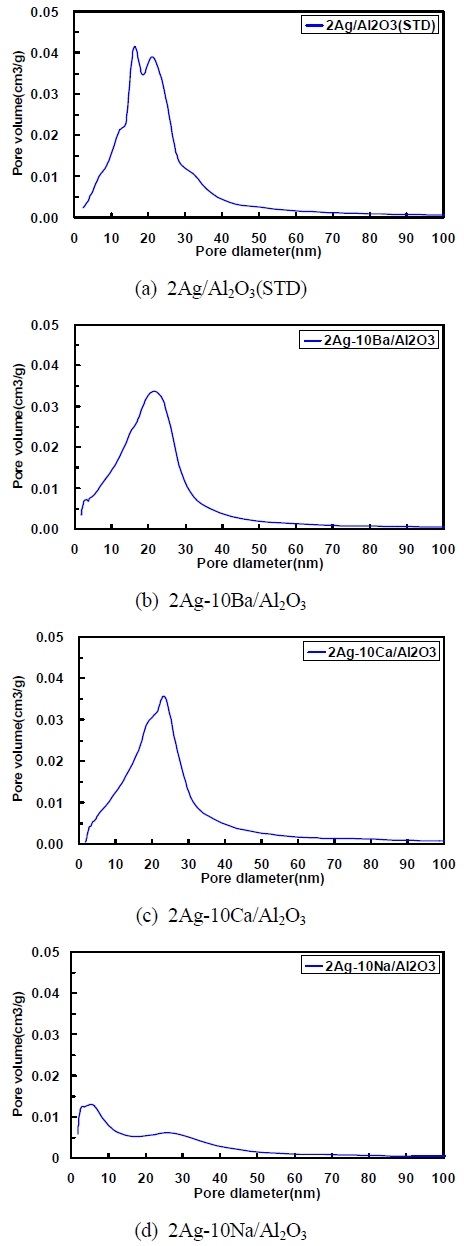
Fig. 3은 알칼리 금속 담지에 따른 H2-SCR의 BJH-Plot를 나타내고 있다. BJH-Plot은 촉매의 meso/macro 세공(pore) 크기 분포를 나타내는 분석이다. 2Ag/Al2O3(STD) H2-SCR은 약 18∼22 nm급의 세공들이 잘 발달되어 있고 Pore volume도 높다. Ba와 Ca가 담지된 두 종류 H2-SCR은 유사한 수준의 약 22 nm급의 세공들이 분포되어 있다. 그러나 2Ag-10Na/Al2O3 H2-SCR 약 10 nm급 이하의 세공들이 형성되어 있으며, Pore volume 값이 급격히 저하되었다.
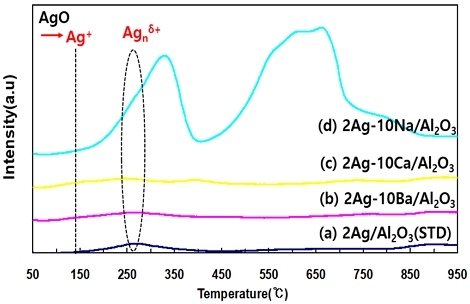
Fig. 4는 네 종류의 H2-SCR의 H2-TPR 피크를 나타내고 있다. 실험 조건은 500℃에서 3시간 동안 공기에서 소성(calcination)한 촉매 파우더에 BEL-CAT(H2-TPR) 분석기를 이용하여 H2 5%/Ar을 50∼1,000℃까지 분당 10℃ 상승시켜 거동을 파악하였다. Fig. 4(a)는 2Ag/Al2O3(STD) H2-SCR은 500℃에서 소성된 주촉매 Ag는 AgO가 된다. H2-TPR 실험에서 환원되는 피크는 약 140℃에서는 Ag+로 환원된다. (a) 2Ag/Al2O3(STD) H2-SCR은 약 260℃에서 환원되는 피크가 발생되며, AgO은 산화물에서 Agnδ+로 환원되었다. Ag 클러스터(Agnδ+)는 AgO 산화물보다 불안정한 상태이므로 Ag의 촉매의 화학 반응을 촉진시킬 수 있다. Ba와 Ca가 담지된 두 종류 H2-SCR은 H2-TPR 피크가 완만하여 환원된 Ag 화학종을 판단하기 쉽지 않다. 그러나 (d) 2Ag-10Na/Al2O3 H2-SCR 약 320℃와 650℃에서 환원 피크가 잘 형성되며, 이는 알칼리 금속 Na가 NaO 산화물로 존재하다가 H2-TPR에 의해 환원되는 피크라고 판단한다.
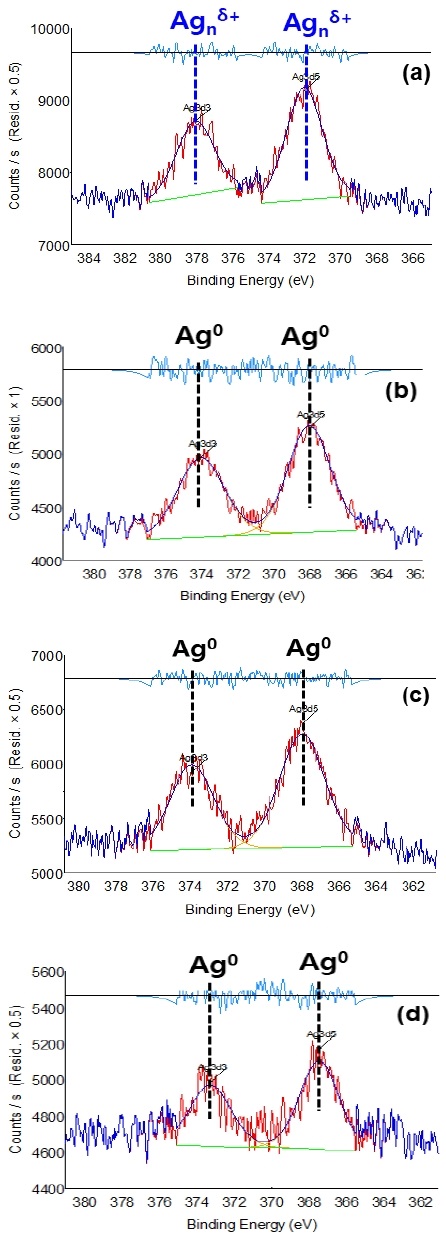
Fig. 5는 Ag 기반 알칼리 금속 담지에 따른 XPS spectra를 보여 주고 있다. Ag는 350∼380eV F영역대의 피크에서 확인할 수 있다. (a) 2Ag/Al2O(STD) H2-SCR은 Ag 담지량이 많아짐에 따라 377.7, 371.6ev에서 주 피크를 확인할 수 있다. 이 주 피크는 Ag 클러스터(Agnδ+)로 Ag가 형성되었음을 확인할 수 있다. 알칼리 금속이 담지된 세 종류 H2-SCR은 374.4, 368.4 ev에서 주 피크를 확인할 수 있다. 이 영역대에서 생성된 피크 Ag0 화학종으로 양이온 또는 음이온으로 형성된 전자가는 촉매활성을 촉진시킬 수 있으나, 중성을 띤 Ag0는 화학반응을 할 때 촉매활성이 저하된다.
3.2 H2-SCR의 알칼리 금속 담지에 따른 유해가스 저감 특성
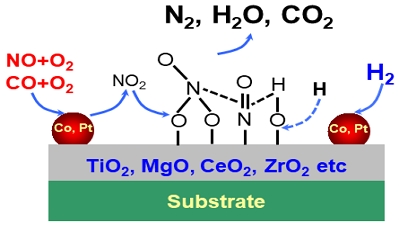
Fig. 6은 H2-SCR의 유해가스 NOx, CO의 동시저감 메커니즘을 나타내고 있다. 소량의 귀금속 Pt는 O2가 있는 분위기에서 NO와 CO를 산화시키며, NO는 질산염(nitrate)으로 흡장된 뒤 환원제 H2가 공급될 때 환원된다. 환원제 H2는 저온에서도 spillover가 되므로 NOX를 저감시킬 수 있다. NO와 CO의 산화와 환원 반응식을 (2)~(6)에 나타내었다.
| (2) |
| (3) |
| (4) |
| (5) |
| (6) |
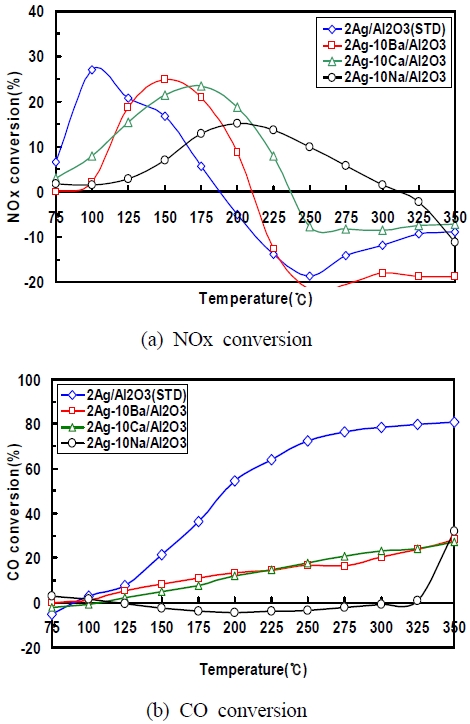
Fig. 7은 H2-SCR의 알칼리 금속 담지에 따른 유해가스 저감 성능을 나타내고 있다. 2Ag/Al2O3(STD) H2-SCR은 100℃에서 약 27%의 NOx 전환율을 나타내며, 약 200℃에서는 (-) NOx 전환율을 나타내고 있다. 온도가 상승하면 환원제 H2는 산화됨에 따라 일반적으로 중·고온에서는 NOx 저감 성능이 저하된다. H2-SCR 촉매 전단에 유입되는 500 ppm NO 가스는 환원되지 않으며 NO2 가스가 증가하므로 (-) NOx 전환율을 나타낸다. 2Ag-10Ba/Al2O3 H2-SCR은 125℃에서 약 19%, 150℃에서 약 25%의 NOx 저감 성능을 나타내고 있다. 2Ag-10Ca/Al2O3 H2-SCR은 100℃에서 약 8%, 175℃에서 약 24%의 NOx 저감 성능을 나타내고 있으며, 250℃에서 (-) NOx 전환율을 나타내고 있다. 2Ag-10Na/Al2O3 H2-SCR 촉매는 175℃에서 약 14%, 200℃에서 약 15%의 가장 낮은 NOx 전환율 을 나타내고 있다. 이는 Table 2에서 볼 수 있듯이 네 종류 H2-SCR 중에서 BET 비표면적과 Pore volume이 가장 작으므로, 이는 촉매 활성사이트 감소로 인하여 NOx 전환율이 저하되는 것이다.
Fig. 7(b)는 CO 전환율을 나타내며, 2Ag/Al2O3(STD) H2-SCR은 촉매온도 125℃에서 약 8%, 온도가 상승하면서 활성화 에너지가 더 많이 공급되면서 350℃에서 가장 높은 약 82%의 CO 전환율 나타내고 있다. Ag 기반의 H2-SCR은 귀금속 Pt와 Pd 기반의 H2-SCR 촉매보다 전반적으로 NO와 CO 전환율 성능이 낮고, 저온 활성도 저하되는 문제는 촉매 물질 Ag가 가지고 있는 특성이기 때문이다. Ba와 Ca가 포함된 두 종류 H2-SCR은 CO 전환율 성능이 낮고, 350℃에서 약 30%의 CO 전환율을 나타내고 있다. 2Ag-10Na/Al2O3 H2-SCR은 350℃을 뺀 나머지 75∼325℃ 온도에서 CO 전환율은 “0”에 가깝다. 이는 NaO 산화물 양 증가로 인해 BET 비표면적의 급격한 감소로 활성사이트가 감소하였고, 더불어 Ag0 화학종이 활성적이지 못하기 때문이다.
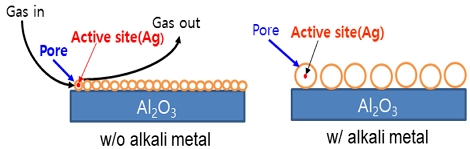
Fig. 8은 알칼리 금속 담지에 따른 H2-SCR의 Pore size와 BET 표면적의 관계를 도식화하였다. 알칼리 금속이 담지 되지 않은 좌측 그림은 작은세공이 잘 발달되어 BET 비표면적이 크고, Pore vloume 값도 커진다. 세공 내에 활성물질인 Ag가 잘 담지되면 유해 가스가 세공 내 활성물질을 통할 때 흡착-반응-탈착의 화학반응이 일어나 유해가스를 저감시킨다. 그러나 우측 그림처럼 알칼리 금속 담지로 인하여 세공 사이즈가 커지면 BET 비표면적과 Pore volume값이 전체적으로 작아지므로 인하여 촉매의 활성은 저하되는 것이다.
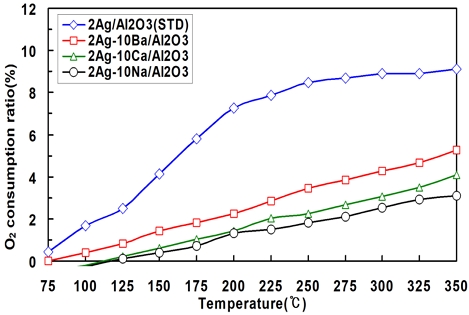
Fig. 9는 알칼리 금속 담지에 따른 NOx와 CO가 저감될 때 얼마나 O2가 소모되었는지를 가늠하는 O2 소모율을 나타내고 있다. 2Ag/Al2O3(STD) H2-SCR은 Fig. 7에서 볼 수 있듯이 네 종류 촉매 중에서 가장 유해가스 저감 성능이 우수한 H2-SCR이다. 100℃에서 약 8%, 350℃에서 약 9% 수준의 O2를 소모하였다. 이는 H2가 NOx 환원과 CO 산화에 사용되었기 때문이다. 알칼리 금속 Ba와 Ca가 담지된 두 종류 H2-SCR은 350℃온도에서 최고 5.5%, 4% 수준으로 O2가 소모되고 있으며, 알칼리 금속이 담지되지 않은 H2-SCR 보다 작다. NOx와 CO 저감 성능이 가장 저하된 2Ag-10Na/Al2O3 H2-SCR은 O2 소모율이 가장 작고, 350℃에서 약 3.2%를 나타내고 있다. 유해가스 저감 성능과 O2 소모율은 상관관계가 성립된다고 할 수 있으며, 이는 H2-SCR은 CO 산화와 NOx 환원이 동시에 일어나는 촉매로써 유해가스를 동시에 저감시키기 위해서는 그만큼 O2 소모량이 증가하기 때문이다. 유해가스 NOx와 CO가스를 저감시키기 위해서는 알칼리 금속이 담지될 경우 촉매 활성이 저하되면서 유해가스 전환율 window가 우측으로 이동하였다. 자동차용 H2-엔진용이나 배출가스가 낮은 가정·산업용 보일러용에 따라 H2-SCR에는 다른 촉매물질 구성으로 유해가스 저감 성능을 향상할 필요가 있다.
4. 결 론
H2-SCR에 알칼리 금속이 담지에 따른 유해가스 저감 특성을 파악한 결과는 다음과 같다.
1) H2-SCR에 NOx 흡장 물질을 담지하면 BET 비표면적이 작아짐에 따라 촉매의 활성 사이트가 감소하여 유해가스 저감 성능이 저하되었다.
2) 2Ag/Al2O3(STD) H2-SCR은 약 260℃에서 AgO 산화물에서 Agnδ+로 환원되었다. Ag 클러스터(Agnδ+)는 AgO 산화물보다 불안정한 상태이므로 Ag의 촉매의 화학 반응을 촉진시켰다.
3) 2Ag/Al2O3(STD) H2-SCR은 125℃ 이하 온도에서 알칼리 금속이 담지된 세 종류 H2-SCR보다 활성화 되었다. 알칼리 금속 담지는 NOx 흡장량 증가를 통하여 NOx 저감 성능에 미치는 영향은 나타나지 않았다.
4) 알칼리 금속이 담지된 세 종류 H2-SCR은 O2 소모율이 작은 경향을 나타냈고, 산화와 환원 반응이 동시에 일어나는 특성에 따라 O2 소모율이 증가할수록 유해가스 저감 성능이 증가하였다.
Acknowledgments
이 연구는 호원대학교 교내연구비로 수행되었으며 지원에 감사드립니다.
Author contributions
C. K. Seo; Conceptualization. Data curation. Investigation. Project adminstration. Writing-original draft. Writing-review & editing.
References
- KIEP, 2021, “International Community’s Carbon Neutral Policy Direction and Implications”, World Economy Today, 21(1).
- Association for Emissions Control by Catalysis (AECC), 2020, “EURO 7/Ⅶ Emission Standards”, AECC position paper.
- WHO Global Air Quality Quidelines, 2021.
-
C. K. Seo and K. S. Lee, 2021, “Characteristics of Exhaust Emissions Conversion of Commercial Cu-and Fe-SCR Catalysts”, International Journal of Automotive Technology, 21(6), 1401-1408.
[https://doi.org/10.1007/s12239.020.0132.6]

-
X. Zhang, X. Zhang, X. Yang, Y. Chen, X. Hu and X. Wu, 2021, “CeMn/TiO2 Catalysts Prepared by Different Methods for Enhanced Low-Temperature NH3-SCR Catalytic Performance”, Chemical Engineering Science, 238, 116588.
[https://doi.org/10.1016/j.ces.2021.116588]

-
C. N. Costa and A. M, Efstathiou, 2007, “Mechanistic Aspects of the H2-SCR of NO on a Novel Pt/MgO-CeO2 catalyst”, The Journal of Physical Chemistry C 111, 7, 3010-3020.
[https://doi.org/10.1021/jp064952o]

-
K. Yokota, M. Fukui and T. Tanaka, 1997, “Catalytic removal of Nitric Oxide with Hydrogen and Carbon Monoxide in the presence of Excess Oxygen”, Applied Surface Science, 121-122(2), 273-277.
[https://doi.org/10.1016/50169-4332(97)00305-X]

-
R. Burch and M. D. Coleman, 2002, “An Investigation of Promoter Effects in the Reduction of NO by H2 under Lean-Burn Conditions”, Journal of Catalysis, 208(2), 435-447.
[https://doi.org/10.1006/jcat.2002.3596]

-
G. J. Kim, J. H. Shin, S. B. Kim and S. C. Hong, 2023, “The Role of Pt Valence State and La Doping on Titanium Supported Pt-La/TiO2 Catalyst for Catalytic Reduction with H2”, Applied Surface, Science, 608, 155040.
[https://doi.org/10.1016/j.apsusc.2022.155040]

-
L. Cao, Q. Wang and J. Yang, 2020, “Ultrafine Pt Particle Directed by Polyvinypyrrolidone on Zeolite Beta as an Efficient Low-Temperature H2-SCR Catalyst”, Environmental Chemical Engineering, 8(1), 103631.
[https://doi.org/10.1016/j.jece.2019.103631]